Curva de presión de vapor y diagrama de fases del agua
| Experimento - Medios didácticos para experimentar/El calor de evaporación/Curva de presión de vapor y diagrama de fases del agua | |
|---|---|
| (Selecciona [Contraer] para reducir el recuadro, [Expandir] para ver contenido no mostrado). | |
| Autor | MediaHouse GmbH |
| Área | Ciencias Naturales |
| Nivel y/o grado | Básico
|
| Tipo de licencia | CC BY-SA |
| Formato | pdf, doc |
| Responsable de curación | Editor |
| Última actualización | 2018/08/01 |
| Localización | https://medienportal.siemens-stiftung.org/es/experimento-10-a4-el-calor-de-evaporacion-107372 |
Por favor, califica el recurso solo si lo has revisado y/o o usado.
Descripción del recurso[editar | editar código]
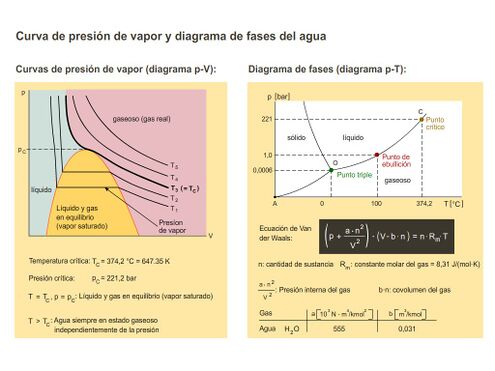
Si se calienta agua a 100 °C a presión atmosférica normal, ésta se convierte en vapor. Pero, ¿qué efecto tiene aumentar o disminuir la presión sobre la temperatura de vaporización?
La curva de presión de vapor (curvas T en el diagrama p-V a la izquierda) y el diagrama de fases (diagrama p-T a la derecha) contestan dicha pregunta. La presión de vapor es la presión a la cual la fase líquida y gaseosa están en equilibrio, es decir, el mismo número de moléculas que se evaporan se condensan nuevamente. Por encima de la temperatura crítica (se dan valores numéricos) el agua es siempre gaseosa, independientemente de la temperatura, y se la puede tratar como un gas real (ecuación de Van der Waals, fórmula provista). Para cada temperatura por debajo de la temperatura crítica hay una presión de vapor para la cual hay una zona bifásica (líquida y gaseosa). Se puede deducir, a partir del aumento pronunciado en las curvas en el intervalo de la fase líquida, que las sustancias líquidas son apenas compresibles. No se ha de confundir la temperatura crítica con la temperatura del punto triple (véase el diagrama p-T). Esto caracteriza los valores de temperatura y presión a los cuales todas las fases (sólida, líquida y gaseosa) están presentes simultáneamente.
Información e ideas:
¿A qué temperatura hierve el agua en el Monte Everest? Las “tablas de presión de vapor” proveen información sobre esto. También sería interesante referirse a los puntos de transición de fases como puntos críticos de temperatura. En la transición de la fase líquida a la gaseosa la energía aplicada no causa inicialmente un aumento de la temperatura. Lo mismo es pertinente a la fusión del hielo. No es sino hasta que toda el agua se ha evaporado o fundido que la temperatura aumenta.
Comentarios adicionales[editar | editar código]
©Siemens Stiftung 2018, Contenido licenciado bajo CC BY-SA 4.0 internacional